Como muchas otras organizaciones humanitarias, MSF es consciente de que la calidad de los medicamentos y otros productos médicos no siempre está debidamente garantizada en el mercado mundial<p><a href="https://apps.who.int/iris/bitstream/handle/10665/330145/9789241517034-eng.pdf?sequence=1&isAllowed=y"><span style="font-size: 11.0pt; line-height: 107%; font-family: 'Calibri',sans-serif; mso-ascii-theme-font: minor-latin; mso-fareast-font-family: Calibri; mso-fareast-theme-font: minor-latin; mso-hansi-theme-font: minor-latin; mso-bidi-font-family: Arial; mso-bidi-theme-font: minor-bidi; mso-ansi-language: EN-US; mso-fareast-language: EN-US; mso-bidi-language: AR-SA;">Hoja de ruta para el acceso a medicamentos, vacunas y otros productos sanitarios 2019-2023, OMS </span></a></p>. El equipo de coordinación de la Oficina Internacional de Garantía de Calidad (IO QA) ha desarrollado tres esquemas de calificación para la aprobación interna de:
- medicamentos
- productos sanitarios, diagnósticos in vitro y artículos de laboratorio; y
- alimentos terapéutcos especializados.
Principios:
- La calificación es un procedimiento estandarizado de evaluación de la calidad para validar (o no) los productos médicos antes de que puedan adquirirse para su uso por parte de MSF, verificando que el producto cumple al menos las normas de calidad reconocidas internacionalmente. El proceso de calificación consiste en la evaluación del expediente del producto y del lugar de fabricación (por ejemplo, una auditoría de Buenas Prácticas de Manufactura, BPM).
- Los procedimientos de calificación de MSF se basan en la confianza mutua. Se pide al fabricante que certifique la veracidad y exactitud de la información y los documentos presentados a MSF. Los errores u omisiones pueden llevar a la descalificación del producto y/o del fabricante.
- Los esquemas de calificación de MSF no pretenden interferir con la iniciativa de precalificación de la Organización Mundial de la Salud (OMS), ni duplicar ningún trabajo existente llevado a cabo por el grupo de autoridades reconocidas como SRA (Stringent Regulatory Authority) por la OMS. Por lo tanto, cualquier producto médico precalificado por la OMS o fabricado y registrado y /en el mercado de una autoridad reconocida como SRA por la OMS es automáticamente calificado por MSF.
- MSF no es una Agencia Reguladora ni un organismo certificador. El sistema de calificación de MSF ha sido diseñado exclusivamente para MSF y las decisiones tomadas sólo son válidas para MSF. Las decisiones se toman utilizando un sistema de calificación predefinido, para garantizar la imparcialidad.
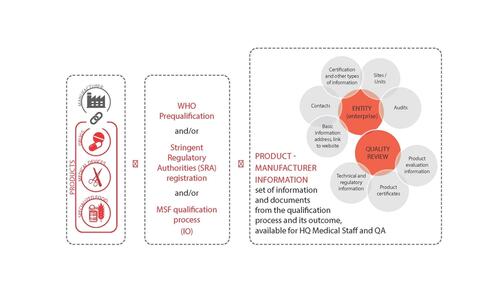
Método
Las diferentes etapas del proceso se basan en lo siguiente:
- Pre-evaluación basada en el cuestionario del producto y/o del fabricante.
- Buenas Prácticas de Manufactura (BPM): inspección del lugar de fabricación: la evaluación del cumplimiento por parte del centro de producción de las Buenas Prácticas de Manufactura (BPM) es el primer paso necesario dentro de la evaluación. Para las medicinas, sólo serán evaluados productos fabricados en una planta de fabricación que cumple con las BPM de acuerdo con la OMS. Las inspecciones de BPM conducidas por el programa de precalificación de la OMS (WHO PQ) o cuerpos de inspectores reconocidos por MSF son tomados en consideración por MSF. Para fábricas que no han sido previamente inspeccionadas y aprobadas por la OMS (WHO PQ) o un cuerpo de inspectores de una autoridad reconocida como SRA por la OMS, el Coordinador Internacional de Garantía de Calidad de MSF designará a un experto en BPM para realizar la inspección.
- Evaluación del producto: para medicinas, la evaluación se basa en el cuestionario de producto/fabricante, de acuerdo a los estándares definidos por la OMS, y basado en un cuestionario estándar común al Grupo de Farmacéuticos Interagencia (UNICEF, CICR, El Fondo Mundial, centro de compras de la OMS, FNUAP, GDF y MSF).
- Control y seguimiento activos
Procesos de calificación de MSF

Proceso de calificación de medicamentos de MSF

Proceso de calificación de MSF de dispositvos médicos y diagnósticos in vitro
Proceso de calificación de MSF para alimentos para fines medicinales especiales
Si la evaluación es satisfactoria, se emite una "hoja de especificaciones del producto" (del inglés “Product Specifications Sheet, PSS) que resume las características del producto aprobadas por MSF, y que se utiliza como referencia para la adquisición.
La calificación de MSF es un procedimiento continuo y los productos aprobados se supervisan a intervalos regulares. Las actividades de seguimiento se centran en la reevaluación del cumplimiento de las Buenas Prácticas de Manufactura (BPM) del centro de producción y en la actualización de la información y los datos facilitados en la evaluación del producto.
Expresión de interés
Los fabricantes y proveedores de productos médicos, medicamentos, vacunas, productos terapéuticos especializados, reactivos y equipos de laboratorio, y material y equipos médicos son bienvenidos a expresar su interés en convertirse en proveedores validados por MSF, enviando un correo electrónico al asistente de los coordinadores de garantía de calidad a [email protected]
No se tendrán en cuenta los productos que no figuren en la lista de medicamentos de MSF, la lista de alimentos terapéuticos especializados de MSF o la lista de productos sanitarios de MSF.
Sólo se tendrán en cuenta para la compra los fabricantes cuyos productos hayan sido calificados por MSF.



